Патрон сигнальный ночного и дневного действия - Перхлораты
Патрон сигнальный ночного и дневного действия
Эффективное сигнальное средство, которое используется для сигнала бедствия в любое время суток. Есть в наличии у экипажей самолетов и вертолетов. Специализированный патрон включает в себя корпус, который разделен горизонтальной перегородкой на несколько камер с установленными внутрь сигналами.
Конструкция ночного сигнала включает бумажную трубку с запрессованным составом красного огня. Дневной предусматривает бумажный стакан из 3 шашек с оранжевым дымом и специальной таблетки для воспламенения. Крышка, навинченная на корпус, обладает соответствующим углублением для быстрого опознавания сигнала в темное время суток.
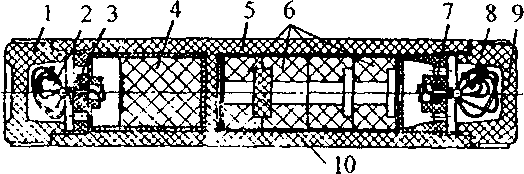
1,9 - крышка; 2, 8 - шнур с кольцом; 3,7- воспламенительное устройство; 4 - пироэлемент ночного сигнала; 5 - корпус; 6 - пироэлемент дневного сигнала; 10 - воспламенительная таблетка
Привести патрон в действие не сложно. При быстром продергивании терки через специализированный капсюль-воспламенитель с использованием шнурка с кольцом она автоматически проходит через имеющийся пиротехнический состав с последующим воспламенением. Возникшее пламя инициирует поджог воспламенительной таблетки и одновременно шашки оранжевого цветового оттенка. Сигнал бедствия в темное время суток подается аналогичным образом.
Важно: длительность сигнала вне зависимости от времени суток составляет от 25 секунд, максимальная дальность – 20 км.
Перхлорат калия
Перхлорат калия изоморфен с перманганатом калия и образует с ним смешанные кристаллы. Полиморфное превращение орторомбической модификации в кубическую происходит при температуре 293-310°С, сопровождается значительным увеличением объема и поглощением тепла 13,76±0,17 кДж/моль. Плотность кубической модификации составляет 2150-2180 кг/м3. П.к. при нормальной температуре слабо растворим в воде, но с повышением температуры растворимость возрастает. Слеживаемость и гигроскопичность чистого П.к. незначительна; наличие примесей повышает последнюю. В органических растворителях П.к. растворяется слабо, он стоек к кислотам. Смеси П.к. с горючими менее чувствительны к тепловым и механическим импульсам, чем смеси на основе хлората калия.
Ускоряют разложение П.к. добавки меди и оксидов марганца, магния, хрома, меди, железа, кобальта, вольфрама, оксид алюминия и карбонат кальция на разложение не влияют. Наиболее высокой каталитической активностью отличается смесь двуокиси марганца и окиси никеля, взятых в соотношении 2:1. Разложение П.к. в присутствии органических горючих и воспламенение смесей горючее-перхлорат калия начинается при температуре 230-290°С, а смесей перхлорат калия-углерод - 300-360°С. Снижают температуру разложения и металлические горючие. Высокое содержание свободного кислорода (46%), малая гигроскопичность и относительно низкая чувствительность смесей на его основе к механическим воздействиям определили широкое использование П.к. в пиротехнических составах различного назначения - осветительных, фотоосветительных, сигнальных, трассирующих, воспламенительных, зажигательных, замедлительных, звуковых.
Перхлорат лития
Как правило, выступает тригидратом. Показатели теплоты приравниваются к 59,41 кДж/моль. При достижении 100С теряет 2 молекулы воды, при 130С формируется безводная соль. В спиртовом растворе и органическом растворителе показатели растворимости П.л. существенно выше, если сравнивать с другими перхлоратами щелочного металла.
Выраженный процесс разложения П.л. становится заметным при достижении температуры, которая выше показателей плавления. Отличительной особенностью П.л. считается высокий уровень содержания активного кислорода (60.1%). Это позволяет снизить уровень окислителя в топливах до 75% включительно с одновременным улучшением технологических свойств. Перхлорат лития:
- не токсичен;
- имеет высокие показатели плотности;
- является термостабильным.
Главный недостаток заключается в высоком показателе молекулярной массы продуктов сгорания. Следовательно, наблюдается существенное снижение удельного импульса. При этом наблюдается повышенная температура продуктов сгорания топлива с содержанием П.л., если сравнивать с аналогичными продуктами, имеющими в составе перхлорат аммония. Дополнительным недостатком считается сложность удаления кристаллизационной воды из него, а также высокие показатели гигроскопичности. Считается дорогостоящим и одновременно дефицитным продуктом, поэтому не используется в производстве пиротехнических средств.
Перхлорат натрия
Обладает соответствующей кубической кристаллической решеткой, является гигроскопичным, отлично растворяется в воде, спирте и ацетоне в частности. При контакте с водой формируется моногидрат, с аммиачным раствором – тетрааммиакат.
На термограммах, которые были получены с использованием метода ДТА, наблюдается выраженный эндотермический эффект полиморфного превращения при показателях 313 и непосредственно плавлений 473С. По достижению температуры 570-640С становится выраженной комбинация эндо и экзотермических процессов.
MnO3 и соответствующая из него смесь с NiO позволяют сдвинуть начало разложения в сторону пониженной температуры (до периода плавления). Принцип подразумевает под собой экзотермический характер. Главными продуктами разложения П.н. выступают NaCl и О2. Продукт часто используется в производстве ракетного топлива, а также многочисленных осветительных и фотоосветительных составах. Широкая сфера применения исключается по причине повышенного показателя гигроскопичности, а также чувствительности смеси к воздействию различных внешних факторов.
Перхлораты
Подразумевают под собой белые либо бесцветные кристаллические компоненты. Обладают ромбической решеткой при нормальном температурном режиме – исключение перхлорат лития, который способен переходить в кубическую.
К сведению: чем выше заявленная масса катиона, тем ниже показатели температуры полиморфного превращения. Перхлорат лития может плавиться при достижении 235-247С, заявленная теплота плавления – 20.3 кДж/моль. Прочие П. не обладают конкретным параметром температуры плавления, поскольку разложение начинается до этого момента. Стремительное разложение наблюдается по завершении плавления, при этом на термограммах выражается экзотермический эффект.
Процесс разложения перхлората лития, натрия, магния, а также соответствующих щелочноземельных металлов становится выраженным при условии выделения тепла в 25-30 кДж/моль. При этом щелочноземельные металлы не обладают полиморфным переходом. В результате процедуры разложения П. бария формируется оксид и хлорид, а также хлор и кислород. Процесс разложения П.м. и свинца образует соответствующий оксид металла, хлора и кислорода в частности.
Добавление многочисленных видов органического горючего влечет стремительное падение температуры с последующим разложением перхлората. Процесс сопровождается выделением существенного объема тепла. Активное взаимодействие П. калия, натрия и бария непосредственно со сплавом АМ инициируется при условии достижения температуры в 464С – исключительно после плавления.